Dividimos la materia en tres estados. Sólido, líquido y gaseoso. ¿Pero que los distingue? ¿Qué hace que el agua sea sólida o gaseosa? La respuesta es la ordenación de los átomos.
En la materia, a nivel microscópico, la estructura es la forma en la que se colocan los átomos. Cuando están desordenados, decimos que la materia está en estado gaseoso. Cuando los átomos se colocan formando una estructura compacta, lo llamamos sólido o cristalino.

Esta estructura no se forma al azar. Sino que toma una forma poligonal y la repite periódicamente a lo largo y ancho del sólido. Existen varias formas geométricas para la formación de estas estructuras cristalinas. A su representación la denominamos maya o red y la forman vértices y aristas que definen las caras de los poliedros de la red. Los átomos pueden situarse tanto en los vértices como en el punto medio de las aristas o en el centro de las caras. Pero todas tienen en común que son la distribución que hace que los huecos entre los átomos sea mínimo.
Esto quiere decir que si suponemos que los átomos son pelotas que metemos en una caja, estos se ordenarán de forma que puedan entrar el mayor número de pelotas en la caja.
Si seguimos con el ejemplo de la caja, con las pelotas bien colocaditas, y unimos el centro de todos los átomos por líneas imaginarias podemos ver una red estructurada. En la actualidad hay una rama entera de la Física, la del estado sólido, que se dedica a analizar las estructuras en las que se ordenan los sólidos y las propiedades que les confiere. Pero fue en la primera mitad del siglo XIX cuando se empezó a analizar en profundidad estas redes.
El científico que dio con la clave fue el francés Auguste Bravais. Él y los científicos de la época, primero decidieron que había que clasificar las redes. Pero se dieron cuenta de que no todas formaban redes polinómicas sencillas. Por lo que había que buscar una definición sobre la que basar las diferentes estructuras.

En algunos casos calcular la celda unidad era sencillo, pero en otras estructuras más complejas con celdas no paralelepípedas, no era tan sencillo. De esta forma desarrollaron un método para obtener la celda unidad o primitiva, que constituye la base de la red. Ya que su repetición, ya sea en el plano o en el volumen, cubre todo el espacio de forma idéntica.
Por lo que para obtener dicha celda primitiva hay que unir un punto del átomo o molécula con el mismo punto de los elementos vecinos. Estos vecinos son los que están más próximos a la partícula base en cualquier dirección, no hace falta que se toquen. Una vez hechas estas líneas trazamos las mediatrices. Estas son las rectas tangentes, con ángulos en la intersección de 90º, que pasan por el punto medio de cada línea de unión. Todas estas mediatrices terminan cortándose entre ellas formando un polígono cerrado con la partícula en el centro. Este polígono es la celda primitiva de la red o celda de Wigner–Seitz.
Bravais se dio cuenta de que en un sólido cristalino solo se podían encontrar 14 tipos de celdas primitivas. Y que con estas podían representarse todas las estructuras cristalinas. Por esta razón las primitivas son denominadas Redes de Bravais.
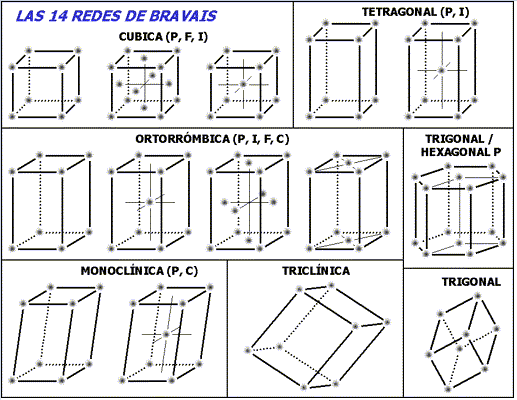

Las redes en el plano están definidas por los ángulos de intersección de las aristas. Oblicua, cuadrada, hexagonal, rectangular y rectangular centrada.
Mientras que las definida en el espacio tridimensional tienen varias clasificaciones. Por un lado se dividen según la forma polinómica, y por otro, la posición que ocupan las partículas en la red. El número de átomos por celda, el factor de empaquetamiento (porcentaje de espacio ocupado en la red) o número de coordinación (número de átomos en contacto con la red) son parámetros característicos de las redes de Bravais.
Por otro lado la clasificación en función de la posición de las moléculas es Cúbica simple (CS), Cúbica centrada en el cuerpo (BCC), Cúbica centrada en las caras (FCC), Hexagonal Simple (HS) y Hexagonal compacta (HCP).
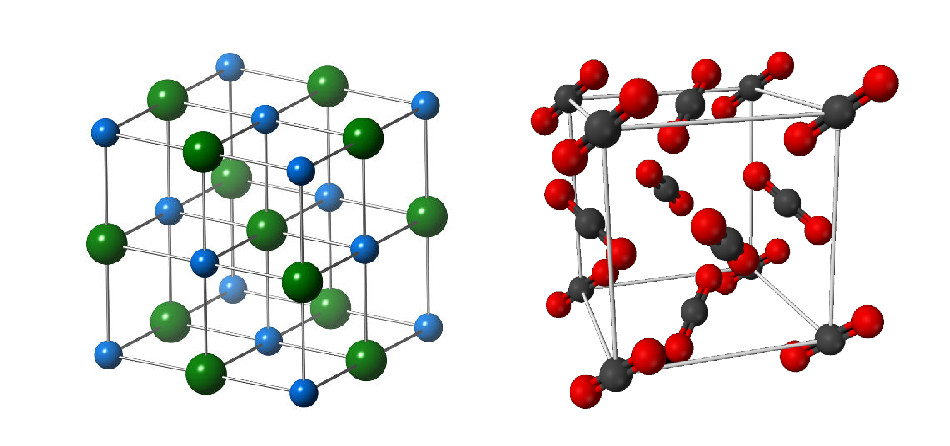
Cuando la estructura cristalina está formada por una sola molécula, todas las posiciones de la red las ocupan los átomos de esta. Si por el contrario la molécula es compuesta, pueden ocurrir dos cosas. Que unas posiciones estén ocupadas por un átomo y otras por otro alternamente, como en el caso del cloruro de sodio, NaCl. Por otro lado se puede dar el caso de que uno de los átomos forma parte de la red mientras que el otro esté desplazado en alguna dirección, pero de forma conjunta. Depende de los enlaces de coordinación que tenga la molécula.
Con las redes de Bravais como base, surgieron una serie de fórmulas que describían a la perfección muchas de las características físicas y químicas de los elementos. Las operaciones de simetría, traslación o rotación de la red determinan propiedades de los sólidos. Y junto con los índices de Miller, que definen los planos cristalográficos de forma unívoca, y que se habían presentado unos pocos años antes, la descripción de los sólidos se formalizó.
Referencias:


